Javaslat a kémiában jelenleg használt szerkezeti képleteknek a térbe való kiterjesztésére, továbbá egy ezzel kapcsolatos megjegyzés a szerves vegyületek optikai forgatóképessége és kémiai konstitúciója közötti összefüggésrôl
1874. szeptember
Forrás: Henry Marshall Leicester, Herbert S. Klickstein: A Source Book in Chemistry, 1400-1900 (Harvard University Press, Cambridge, Massachusetts, 1963)
Elô kívánok vezetni néhány megjegyzést, amelyek vitát válthatnak ki, és remélem, hogy a vita kapcsán határozottabban és bôvebben is kifejthetem nézeteimet. Minthogy a következô közlemény kiinduló pontja a szénvegyületek kémiájában lelhetô fel, egyelôre csupán az erre vonatkozó megállapításokat fogom közölni.
Egyre inkább úgy tûnik, hogy a jelenlegi konstitúciós képletekkel nem magyarázhatók az izoméria egyes esetei; ennek talán az az oka, hogy az atomok aktuális helyzetérôl határozottabb kijelentést kell tennünk.
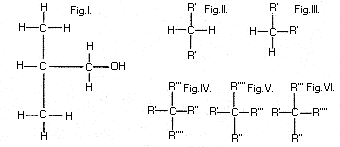
Ha feltesszük, hogy az atomok egy síkban fekszenek, mint
például az izobutil-alkoholban (Fig. I.), ahol a négy
affinitást [vegyértéket] négy olyan vonal jelzi
ebben a síkban, amelyek két, egymásra merôleges
irányt foglalnak el, akkor a metánból (CH4)
hogy a legegyszerûbb esettel kezdjük a következô
izomer alakok származhatnak (a különbözô hidrogénatomokat
egymás után az R', R'' stb. egy vegyértékû
csoportokra cseréljük le):
| CH3R' | és | CHR'3 | egy |
| CH2R'2
CH2R'R'' |
és |
(Fig. II., III.),
CHR'2R'' |
kettô |
| CHR'R''R''' | és | CR'R''R'''R''''
(Fig. IV., V., VI.) |
három |

ezek a számok pedig sokkal nagyobbak, mint az eddig ismert aktuális számok.
Az elmélet összhangba kerül a tényekkel, ha feltesszük, hogy a szénatom affinitásai egy olyan tetraéder csúcsai felé mutatnak, amelynek közepén maga a szénatom van.
Az izomerek száma ekkor csökken, és a következôképpen
alakul:
| CH3R', CH2R'2, CH2R'R'', CHR'3 és CHR'2R'' | egy |
| CHR'R''R''' vagy általánosabban CR'R''R'''R'''' | kettô |
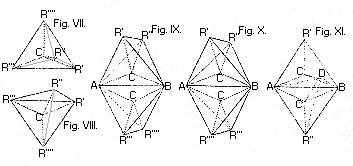 Ha valaki a VII.
és VIII. ábra R'R''' vonalára képzeli magát
úgy, hogy R'-vel szemben áll, és az R''R'''vonal felé
néz, akkor R'' jobbra (Fig. VII.) vagy balra (Fig. VIII.) eshet
a megfigyelôtôl; más szóval: Ha a szénatom
négy affinitását négy különbözô
egy vegyértékû csoport elégíti ki, kettô
és kettônél nem több különbözô
tetraéder adódik úgy, hogy az egyik a másik
tükörképe, és a kettô nem hozható
fedésbe; vagyis két szerkezeti képletet kapunk, amelyek
térbeli izomerek. Eszerint a hipotézis szerint a CR'R''R'''R''''
kombináció olyan állapotot jelent, amelyet sem a CR'2R''R''',
a CR'3R'' vagy a CR'4 kombináció, sem
a szokásos jelölési mód nem ír le. A jelen
reprezentáció szerint a CR'R''R'''R'''' és a CR'2R''R'''
között ugyanakkora a különbség, mint a CR'2R''R'''
és a CR'3R'', vagy a CR'3R'' és a CR'4
között.
Ha valaki a VII.
és VIII. ábra R'R''' vonalára képzeli magát
úgy, hogy R'-vel szemben áll, és az R''R'''vonal felé
néz, akkor R'' jobbra (Fig. VII.) vagy balra (Fig. VIII.) eshet
a megfigyelôtôl; más szóval: Ha a szénatom
négy affinitását négy különbözô
egy vegyértékû csoport elégíti ki, kettô
és kettônél nem több különbözô
tetraéder adódik úgy, hogy az egyik a másik
tükörképe, és a kettô nem hozható
fedésbe; vagyis két szerkezeti képletet kapunk, amelyek
térbeli izomerek. Eszerint a hipotézis szerint a CR'R''R'''R''''
kombináció olyan állapotot jelent, amelyet sem a CR'2R''R''',
a CR'3R'' vagy a CR'4 kombináció, sem
a szokásos jelölési mód nem ír le. A jelen
reprezentáció szerint a CR'R''R'''R'''' és a CR'2R''R'''
között ugyanakkora a különbség, mint a CR'2R''R'''
és a CR'3R'', vagy a CR'3R'' és a CR'4
között.
Ezen hipotézis elsô eredményét a tényekkel összevetve úgy vélem, jó okunk van azt állítani, hogy bizonyos kombinációk, amelyekben egy szénatom négy különbözô, egy vegyértékû csoporthoz kapcsolódik (ettôl kezdve ezen szénatomokat aszimmetrikus szénatomoknak nevezzük), olyan anomáliákat mutatnak az izoméria és egyéb tulajdonságok tekintetében, amelyeket az eddig alkalmazott konstitúciós képletek nem jeleznek.
Elsô rész
I. Az aszimmetrikus szénatom és az optikai aktivitás tulajdonsága közötti kapcsolat
(a) Mindazon szénvegyületek, amelyek oldatban elforgatják a polarizált fény síkját, aszimmetrikus szénatommal rendelkeznek.
Abból a célból, hogy meggyôzôdjünk a megjegyzés igazságáról, végig kell szaladnunk az optikailag aktív vegyületek következô listáján. A képletekben az aszimmetrikus szénatomot C jelöli:
etilidén-tejsav: CH2C.H.OH.COOH
aszparaginsav: COOH C.H.NH2.(CH2COOH)
aszparagin: COOH C.H.NH2.(CH2CONH2)
almasav: COOH C.OH.H.(CH2COOH)
glutársav: CH2OH C.H.COOH.(CH2COOH)
borkôsav: COOH C.H.OHC.H.OH.COOH
dextróz, levulóz [fruktóz], galaktóz, maltóz
szorbin, eukalin stb.: CH2OH.C.H.OH.(C4H7O4)
mannit, kvercit, pinit: (C4H9O4).C.H.OH.CH2OH
...
Az aktív alkaloidok, fehérjék stb. szerkezetérôl még túlságosan keveset tudunk ahhoz, hogy szerkezetük és a forgatóképesség kapcsolatáról bárminemû következtetést levonjunk.
Ezen szabály alól egyetlen kivételt találtam csak, Chancell aktív propil-alkoholját, de Henniger személyes közlése szerint a viszonylag kis forgatóképesség szennyezések eredménye.
(b) Az optikailag aktív vegyületek származékai elvesztik forgatóképességüket, ha az összes szénatom aszimmetriája megszûnik; ellenkezô esetben általában nem veszítik el ezt a képességet.
Elegendô itt néhány példát felsorolni:
az aktív almasavból keletkezô inaktív malonsav,
fumársav és maleinsav; az aktív borkôsavból
keletkezô inaktív borostyánkôsav és tartronilsav,
az aktív kámforból képzôdô inaktív
cimén stb.
Ellenpéldák a következôk:
aktív almasav az aktív borkôsavból, aktív
borkôsav az aktív laktózból, aktív glükóz
az aktív glikozidokból, aktív nitro-mannit az aktív
mannitból, aktív kámforsav és borneol az aktív
kámforból, aktív sók és észterek
az aktív savakból stb.
c) Ha számba vesszük azon vegyületeket, amelyek aszimmetrikus szénatomot tartalmaznak, látható, hogy az a) ellentettje sok esetben nem igaz, vagyis nem minden vegyület hat a polarizált fényre, amely aszimmetrikus szénatomot tartalmaz.
Ez három oknak tudható be:
1. A vegyületek két izomer inaktív keverékei, amely izomerek egyezô, de ellentétes optikai hatással rendelkeznek, és egyéb tulajdonságaik nagy hasonlósága miatt igen nehezen választhatók el, s eddig nem választották szét ôket.
2. A forgatóképesség vizsgálata hibás vagy azért, mert a vegyületek gyengén oldódnak, vagy azért, mert sok vegyületnek, mint például a mannitnak, kicsi a fajlagos forgatóképessége.
3. Elôfordulhat, hogy az aszimmetrikus szénatom önmagában nem elegendô az optikai aktivitás elôidézéhez; ez utóbbi esetleg nemcsak attól függ, hogy a szénhez kapcsolódó csoportok különbözôk, hanem a csoportok jellege is szerepet játszik.
Bármelyik eset álljon is fenn, a felsorolt tények valószínû kapcsolatot jeleznek a konstítúció és az optikai aktivitás között, ami felhasználható a következô esetekben, ha a meggyôzôbb érvek kudarcot vallanak:
1. Az a vegyület, amelyik elforgatja a polarizált fény síkját, valószínûleg aszimmetrikus szénatomot tartalmaz; ez módot ad arra, hogy válasszunk a lehetséges szerkezetek között, ha a vegyületek szerkezetét nem sikerült pontosan meghatározni.
Például az aszimmetrikus szénatomot tartalmazó
aktív amil-alkoholnak csak ez lehet a képlete:
| CH3 | CHCH2OH |
| C2H5 |
Ezt a képletet Erlenmeyer is javasolta, de más volt a kiindulópontja.
2. Ha egy vegyületnek az eddigiek szerint nincsenek olyan fizikai
izomerei, amelyek a polarizált fényre hatnak, minden valószínûség
szerint nem tartalmaz aszimmetrikus szénatomot. Ez a tény
a lehetséges szerkezeti képletek között is segíthet
dönteni. Például a citromsavnak, amely akonitsavvá
és trikarballilsavvá alakul át, a következô
két képlet egyike felel meg:
| C.H.OH.COOH
| CH.COOH | CH2COOH |
vagy | CH2COOH
| C.OH.COOH | CH2COOH |
A vegyület inaktivitása miatt a második képlet tûnik megfelelôbbnek; az elsô aszimmetrikus szénatomot tartalmaz, ennélfogva azt remélem, hogy az említett savat Frankland és Duppa módszerét követve elôállíthatom oxálsavból és jód-ecetsavból cink segítségével.
3. Végül bizonyos valószínûséggel megállapítható, hogy milyen határon túl jelenik meg a forgatóképesség, vagyis megadhatók azok a legegyszerûbb kombinációk, amelyek aktivitást mutatnak. Például a legegyszerûbb aktív egyatomos [egyértékû] alkohol a következô:
CH3C.H.OH.CH2CH3
A legegyszerûbb aktív egybázisú sav:
CH3C.H.COOH.CH2CH3
A legegyszerûbb aktív kétatomos alkohol:
CH3C.H.OH.CH2OH
A legegyszerûbb aktív telített szénhidrogén:
| CH3 | CHC3H7 |
| C2H5 |
A legegyszerûbb aktív aromás szénhidrogén:
| CH3 | CHC6H5 stb. |
| C2H5 |
Ugyanakkor valószínû, hogy néhány
sor nem rendelkezik optikai aktivitással, mint például
| a normál szénhidrogének: | CH3(CH2)nCH3 |
| a normál alkoholok: | CH3(CH2)nCH2OH |
| a normál savak: | CH3(CH2)nCOOH stb. |
Fölöttébb figyelemreméltó, hogy a fenti feltevések következtében a CHClBrI vegyület valószínûleg két olyan izomerre válik szét, amely hatást fejt ki a polarizált fényre. ...
Második rész
Eddig olyan vegyületek esetében vizsgáltuk meg a hipotézis következményeit, amelyekben a szénatomokat csak egyszeres affinitás egyesíti (néhány aromás anyagtól eltekintve); most a következô meggondolásról kell szót ejtenünk:
 Az új
hipotézis
hatása azokra a vegyületekre, amelyek kétszeresen kötött
szénatomokat tartalmaznak. A kétszeres kötést
két olyan tetraéder reprezentálja, amelynek egyik
éle közös (Fig. IX.). A és B szimbolizálja
a kétszers kötést, R,' R'', R''', R'''' pedig azokat
az egy vegyértékû csoportokat, amelyek a szénatomok
szabadon maradó affinitásait telítik.
Az új
hipotézis
hatása azokra a vegyületekre, amelyek kétszeresen kötött
szénatomokat tartalmaznak. A kétszeres kötést
két olyan tetraéder reprezentálja, amelynek egyik
éle közös (Fig. IX.). A és B szimbolizálja
a kétszers kötést, R,' R'', R''', R'''' pedig azokat
az egy vegyértékû csoportokat, amelyek a szénatomok
szabadon maradó affinitásait telítik.
Ha R', R'', R''', R'''' ugyanazt a csoportot jelöli, csak egyetlen elrendezés képzelhetô el. Ugyanez érvényes, ha R' és R'' vagy R''' és R'''' azonos, de ha R' különbözik R''-tôl, miközben R''' különbözik R''''-tôl, ami nem zárja ki R' és R''', R'' és R'''' azonosságát, akkor két elrendezés is lehetséges (Fig. IX. és Fig. X.); ezekben R' és R'' helyzete különbözô R''' és R'''' helyzetéhez képest. E legfeljebb két alakzat eltérése olyan izoméria esetét jelzi, amilyenre a közönséges képletek nem utalnak.
A tényekre térve, úgy vélem, találkoztam ilyen esetekkel a szerves vegyületek között.
1. A maleinsav és a fumársav izomériájára adott minden magyarázat zátonyra futott (ide számítom a két vegyértékû szénatom feltételezését is, minthogy ez csak a szén-monoxid és a karbil-aminok esetében létezhet nyilvánvaló okból a molekula megkettôzôdése nélkül); ezek a savak valójában megfelelnek a fent vázolt feltételeknek: két kétszeresen kötött szénatom mindegyike két eltérô, egy vegyértékû csoportot (H és COOH) hordoz.
2. A bróm- és izobróm-maleinsav esetében az izoméria magyarazáta ugyanaz, mint az elôbb, csak a fumársav és a maleinsav egyik hidrogénjét kell brómra cserélni.
3. Citra-, ita- és mezakonsav. Ha elfogadjuk, hogy
CH3CHCOOHCH2COOH
felel meg a piroborkôsav képletének, akkor az említett savak képlete csak a következô lehet:
CH2=C.COOH.CH2COOH
CH3C.COOH=CHCOOH
és ha hipotézisem értelmében az utóbbihoz nem tartozik két izomer (valószínûleg az ita- és a citrakonsav), nem adható plauzibilis magyarázat.
4. Szilárd és folyékony krotonsav. A szilárd krotonsav képlete Kekulé szerint kétségtelenül
CH3CH=CHCOOH,
ezért ha a kétféle sav különbségét meg akarjuk magyarázni, a folyékony krotonsavnak nem marad más (így tartják), csak a
CH2=CHCH2COOH
képlet.
De ha figyelembe vesszük, hogy
a) ez a sav KOH-dal megolvasztva, M. Hemilian szerint, csak ecetsavat
ad;
b) az oxidálószerek, ugyancsak az említett szaktekintély
szerint, ecetsavvá és oxálsavvá, az oxálsavból
pedig közvetve szénsavvá alakítják át;
c) 170180 o-on, ismét Hemilian szerint, szilárd
krotonsavvá alakul át, semmi sem szól a CH2=CHCH2COOH
képlet mellett, minden a CH3CH=CHCOOH izomerre utal pontosan
úgy, mint a fumársav és maleinsav esetében.
A CH3CH=CHCOOH képlet valóban kielégíti
azokat a feltételket, amelyeket hipotézisem két izomer
létezéséhez megkövetel: két kétszeresen
kötött szénatom, mindegyik szabad affinitását
két eltérô, egy vegyértékû csoport
telíti, ebben az esetben H és CH3, illetve H és
COOH.
Geuther klór-krotonsavja és klór-izokrotonsavja, amelyek izomériáját eddig a következô képletekkel írták le:
CH2=CClCH2COOH és CH3CCl=CHCOOH,
Froelich szerint naszcens hidrogénnel a 4. pontban tárgyalt savakat adja, ezért mindkét vegyület konstitúciója
CH3CCl=CHCOOH.
Az izomériának ez a példája megerôsíti hipotézisemet.
Harmadik rész
Hátra van azoknak a szénatomoknak a tárgyalása, amelyeket háromszoros kötés egyesít, mint amilyen az acetilénben is elôfordul. Ezt a kombinációt két olyan tetraéder reprezentálja, amelyek három csúcsa vagy egy lapja közös (Fig. XI.). ADB jelöli a háromszoros kötést, az R' és R'' egy vegyértékû csoport pedig a szénatomok fennmaradó affinitását telíti. Az új hipotézis ebben az esetben semmilyen ellentmondásra nem vezet a korábban mondottakkal.
Végezetül meg kívánom jegyezni, hogy
1. az új hipotézis semmit nem hagy magyarázat nélkül, amit világosan megmutatnak a fenti meggondolások;
2. egyes tulajdonságokra és izomerekre, amelyeket a szokásos teóriák nem értelmeznek, ez a tárgyalás némi fényt derít;
3. végül az oldatokban jelen levô aktív vegyületekre, vagyis aktív molekulákra vonatkozó megjegyzéseim kapcsolatban állnak Rammelsberg aktív kristályokra vonatkozó elgondolásaival.
Herschell és Pasteur megfigyeléseit kiterjesztve Rammelsberg úgy tartja, hogy a polarizáció síkjára kifejtett hatás a szilárd testek esetén (vagyis a inaktív molekulekulákat tartalmazó kristályok aktív állapota és az aktív molekulákból álló kristályok inaktív állapota) két olyan kristályforma megjelenésével jár együtt, amelyek egymás tükörképei.
Nyilvánvaló, hogy az aktív kristály molekuláinak elrendezése ugyanaz a probléma, mint az aktív molekula atomcsoportjainak hipotézisem szerint elrendezése. Ebben az elrendezésben sem a Rammelsberg által említett kristályoknak, sem a VII. és VIII. ábrán általánosan jelölt aktív molekuláknak nincs szimmetriasíkjuk.
| ChemoNet, 1998
Vissza |
http://www.kfki.hu/chemonet/
http://www.ch.bme.hu/chemonet/ |