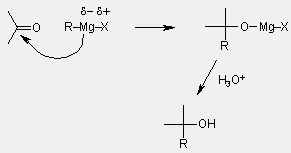9. fejezet
Karbonil-vegyületek
Karbonil funkciós csoportok
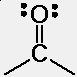
általában két csoportra osztják:
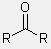 aldehidekre
és ketonokra
aldehidekre
és ketonokra
- mindkét R-csoport lehet C vagy H
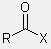 karboxil-származékok
karboxil-származékok
- X: elektronegatív elem
- (halogén, O, N, S stb.)
- a 10. fejezetben tárgyaljuk
A karbonilcsoport - szerkezet és tulajdonság
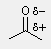
- poláros C=O kettõs kötés
- az O nukleofil
savakkal és elektrofilekkel reagál
- a C elektrofil
Lewis-bázisokkal és nukleofilekkel reagál
Aldehid nómenklatúra
-al utótag, a karbonilcsoport a fõcsoport
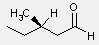 (R)-3-metil-pentanal
(R)-3-metil-pentanal
-formil elõtag
(ha az aldehid nem lehet a fõláncban)
pl. formil-ciklohexán
formaldehid
acetaldehid
propionaldehid
butiraldehid
benzaldehid
Keton nómenklatúra
-on utótag, számmal
 2-hexanon
2-hexanon
-oxo- elõtag, ha szükséges
(ha magasabb prioritású csoport miatt szubsztituensként
kell elnevezni - pl. aldehid esetén)
 5-oxoheptanal
5-oxoheptanal
acil- elõtag
(ha a karbonilcsoport nem része a fõláncnak)
acetil
benzoil
 benzoil-ciklohexán
benzoil-ciklohexán
dialkil-keton
aceton
acetofenon
benzofenon
Nómenklatúra példák
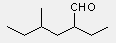 2-etil-4-metil-hexanal
2-etil-4-metil-hexanal
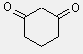 ciklohexán-1,3-dion
ciklohexán-1,3-dion
Aldehid-szintézisek
- primer alkoholok oxidációjával, PCC-vel
Keton-szintézisek
- szekunder alkoholok oxidációjával
KMnO4-tal, CrO3-dal, PCC-vel, Na2Cr2O7-tal
- terminális vagy szimmetrikus alkinek hidratálása
(más alkinek keveréket adnak)
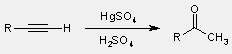
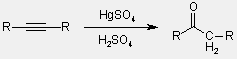
- aromás vegyületek Friedel-Crafts acilezése
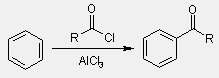
Aldehidek oxidációja
- oxidációra nagyon érzékenyek
(lassú, gyökös mechanizmusú reakció levegõvel)
- Tollen- (ezüst tükör) próba
az Ag+ vizes ammóniában fémezüstté
(tükör) redukálódik
RCHO + Ag+ ——> RCOOH + Ag
Nukleofil addíciók karbonilvegyületekre
a karbonilvegyületek reakciója:
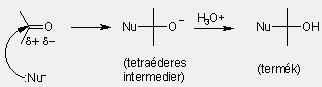
Általános trendek:
- az aldehidek reaktívabbak, mint a ketonok
(sztérikus gátlás a ketonoknál )
- az aromás karbonilok reaktívabbak az alifásoknál
(konjugációs hatás miatt)
- sok nukleofil képes addíciós reakcióra
O nukleofilek: OH-, H2O, ROH
N nukleofilek: NH3, RNH2
H nukleofilek: LiAlH4, NaBH4
C nukleofilek: CN-, RLi, RMgX
Savkatalizált nukleofil addíció
- protonálódással reaktívabb elektrofil keletkezik
(a szénatom könnyebben fogadja a nukleofileket)
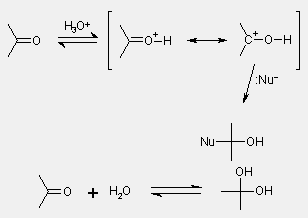
- gyenge nukleofilek esetében jó megoldás
- könnyen protonálódó nukleofilek esetében
nem megy
Hidratáció
- mint a C=C kettõs kötés hidratációjánál,
H és OH kapcsolódik
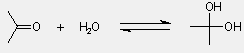
- a H2O nukleofil
- a termék geminális diol
A hidratáció megfordítható egyensúlyi
folyamat
- a formaldehid vízben többnyire dihidroxi-metán
- a legtöbb karbonilvegyület egyensúlya a karbonil forma
felé van eltolódva
(nagyon kevés geminális diol van vizes oldatban)
- pH 7-en a reakció lassú,
de savban vagy bázisban gyorsabb (katalízis)
Báziskatalizált hidratáció
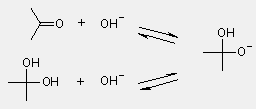
Savkatalizált hidrolízis
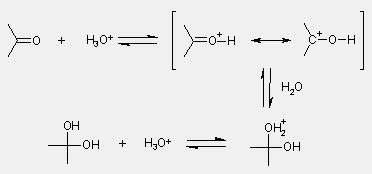
A sav- és a báziskatalízis összehasonlítása
- bázikus közegben deprotonálódással
erõs nukleofil keletkezik
- savban a karbonil érzékenyebbé válik a
gyenge nukleofillel szemben
- egyszerre nem lehet mindkettõ
(habár a természet néhány enzimmel majdnem
ezt teszi)
Alkohol-addíció
- megfordítható folyamatban az általában
nem stabil félacetál keletkezik
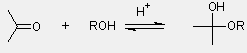 |
| |
félacetál |
- a félacetál savkatalizált szubsztitúciós
reakcióban (SN1) acetállá alakul
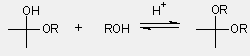 |
| félacetál |
acetál |
- a ketál (és a félketál) kifejezést
gyakran használják a ketonok megfelelõ termékeire
- megfordítható savkatalizált egyensúly
a víz elvonásával eltolható
vízfelesleg hozzáadásával (hidrolízis)
megfordítható
Az acetál mint védõcsoport
- az éter funkciós csoport többnyire nem reaktív
- de könnyedén eltávolítható savas hidrolízissel
- a védõcsoport átmenetileg "elfedi" a
reaktív karbonilcsoportot
- nemkívánt mellékreakciók elkerüléséhez
Amin-addíció
- megfordítható folyamatban az általában
nem stabil aminol keletkezik
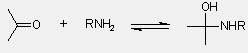 |
| |
aminol |
- az aminol savas katalízissel vizet veszít
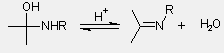 |
| aminol |
imin |
- a savkatalízis csak gyengén savas értéken
megy (tipikusan 4 - 6)
- különben az amin teljesen protonálttá válik,
és úgy nem nukleofil
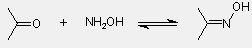 |
| |
oxim |
| |
|
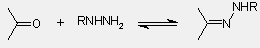 |
| |
hidrazon |
Wolff-Kizsnyer redukció
- karbonilcsoport eltávolító módszer (alkánnál)
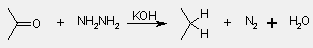
Hidrid-addíció
- redukció LiAlH4-del vagy NaBH4-del ("H-"-addíció)
- irreverzibilis
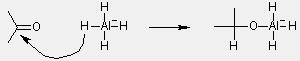
Szénaddíciók
- a cianid-addíció ciánhidrint ad
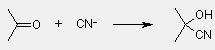 |
| |
ciánhidrin |
- fémorganikus reagensek (nukleofil szén)
- új C-C kötés jön létre, és alkohol
keletkezik
- irreverzibilis
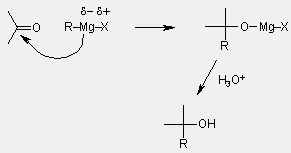
- Grignard + formaldehid --> 1o alkohol
- Grignard + aldehid --> 2o alkohol
- Grignard + keton --> 3o alkohol
- hasznos reakció
új C-C kötés jön létre
hosszabb szénlánc keletkezik
- A Grignard-reagenst a legtöbb funkciós csoport (OH, COOH,
NH2 stb.),
a levegõ nedvessége és oxigénje tönkreteszi
Természetes ciánhidrinek
- néhány organizmus ciánhidrineket használ
védekezési mechanizmusában toxikus HCN kibocsájtására
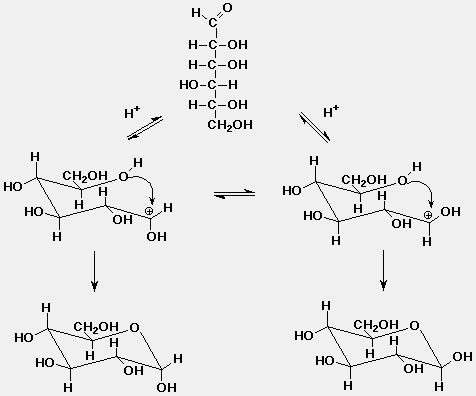
Glükóz félacetálok
- a legtöbb cukor vizes oldatban nagyobb részben gyûrûs
félacetál formában van
Glükóz acetál polimerek (keményítõ
és cellulóz)
- állatokban a glükóz keményítõ
formájában tárolódik,
a növényekben pedig cellulóz a vázanyag
Ismeretanyag
- aldehidek és ketonok elnevezése
- nukleofil addíciós reakció termékének
megadása
- nukleofil addíciós reakció mechanizmusának
felírása
- sav- vagy báziskatalízis hatásosságának
felismerése nukleofil addíciós reakcióban
- Grignard-reakció használata szintézissorokban
- acetál védõcsoport használata szintézissorokban
Vissza
![]()
![]() aldehidekre
és ketonokra
aldehidekre
és ketonokra![]() karboxil-származékok
karboxil-származékok ![]()
(R)-3-metil-pentanal
2-hexanon
5-oxoheptanal
benzoil-ciklohexán
![]() 2-etil-4-metil-hexanal
2-etil-4-metil-hexanal ciklohexán-1,3-dion
ciklohexán-1,3-dion